CMDCAS产品注册
- 立即咨询
-
全国服务热线:
400-888-7587

400-888-7587
♛ 办理介绍 / Introduction
✪ 加拿大医疗器械法规将医疗器械分为I, II,III,IV四个分类,依次依据风险大小,如I类器械为最低风险,IV类器械风险为最高。为此针对制造者提出的产品注册要求也是逐级增加,要求制造者实行的体系是愈加详尽。如I类医疗器械豁免注册。II,III,IV类器械的注册要求如下:
1、通用注册资料:
2、器械的名称;
3、器械的分类;
4、器械的标识;
5、产品标签上出现的制造者名称、地址;
6、若制造地点与d)不同,则制造地名称、地址;
♛ II 类器械注册附加资料:
✪ 所制造、销售或代理的器械关于医用条件的目的及用途的描述;
✪ 为满足安全和有效性要求所符合的标准的清单;
✪ 由制造者的高层主管作的安全有效性符合声明;
✪ 由制造者的高层主管作的器械标签符合加拿大医疗器械法规的声明;
✪ 若是近病人体外诊断设备(即不在医院而是在例如家庭使用的设备),制造者的高层主管应声明已用代表预期使用者的人体物质在与预期使用条件类似的条件下进行了研究性测试;
✪ 由CMDCAS认可机构颁发的CAN/CSA-ISO 13485体系证书。
♛ III类器械注册的附加条件:
✪ 器械及在其制造及包装中所用材料的描叙;
✪ 所制造、销售和代理的器械在其允许的医疗条件、目的和用途下的性能描述;
✪ 除加拿大外的器械获准销售的国家清单、售出数量,以及报导的问题及召回情况;
✪ 器械的设计和制造为满足安全有效性而采用的标准清单;
✪ 如果是以无菌出售的器械,则无菌方法描述;
✪ 制造者为安全有效而进行的研究描述,以及由此得出的结论;
✪ 器械标签/复印件;
✪ 如果为近病人体外诊断设备,用代表目的预期用户的人体物质,以在使用条件类似的条件下的研究测试的情况;
✪ 所有与使用、安全和有效有关的公开发布的报告的文献引用;
✪ 由加拿大医疗器械【信息咨询】机构认可的机构所颁发的CAN/CSA-ISO 13485证书。
♛ IV类医疗器械的附加材料为:
✪ 器械及制造和包装过程中所有材料的描述;
✪ 所制造、销售或代理的器械所允许的医疗条件、目的和用途的器械特性描叙;
✪ 除加拿大以外器械获准销售的国家,售出数量,以及报告器械的问题及召回情况;
✪ 风险评估情况包括风险分析、风险评价,以及评价风险满足安全有效的纠正措施;
✪ 与器械相关的质量计划,如特定的质量实践,资源及行动的程序;
✪ 制造和包装中使用的材料的参数;
✪ 器械的制造过程;
✪ 设计、制造中为满足安全有效要求而采用的标准清单;
✪ 制造者为证明满足安全有效要求而进行的所有研究的详细情况,包括:i) 临床前研究和临床研究; ii) 过程验证研究; iii) 适用时,软件验证研究,和 iv)文献研究;
✪ 若非体外诊断设备、取自动物组织或组织衍生产物的器械,其客观生物安全证据;
✪ 若为近病人体外诊断设备,针对代表预期用户的人体物质且在相似使用条件下进行的研究测试的详细情况;
✪ 制造者依据(i)款研究得出的结论;
✪ 制造者依据(h)款研究的总述及由此得出的结论;
✪ 与器械的使用、安全和有效相关的公开发布报道的文献;
✪ 器械标签的复印件;
✪ 由加拿大医疗器械机构认可的机构所颁发的CAN/CSA-ISO 13485证书。
医疗器械许可证发布后,每年11月1日应由制造者向加拿大卫生部提出再确认。取消生产许可证应在停止加拿大销售的30日之内提出。
㉿ 办理流程 / Processing process
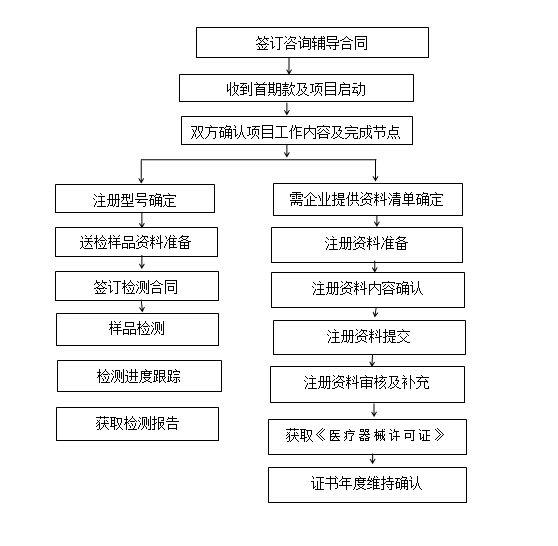
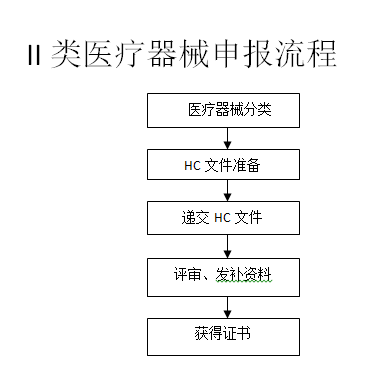
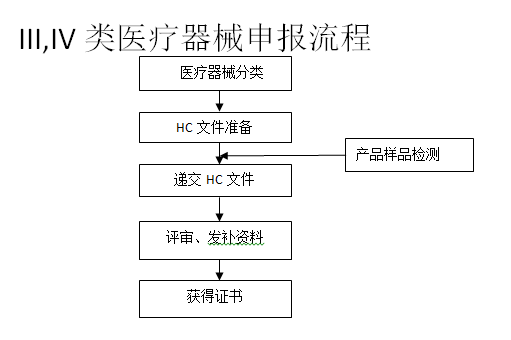
❈ 行政时间 / Administration Service Time
业务名称 | 官方时间 |
II类HC | 90 |
III,IV类HC | 90 |
〠 金飞鹰相关服务 / Golden Eagle related services
● 代表性样检验样品确认
● 样品检验机构确认
● 检验标准确定
● 相关资料合规性审核
● 注册资料编制
● 注册资料提交
● 证书年度维持确认
● 其它必要的工作
全面解决您的研发、生产、验收、营销全流程问题

practical experience
2000多个二、三类医械项目经验沉淀,为你分配做过相同案例的实战老师。
Professional translation
汇聚7大语种专业翻译精英,多年医械行业翻译经验,能准确翻译专业名词及用语。
Software development
强大的软件研发团队,已为集团研发出成熟的项目管理软件,可提供软件定制服务。
Group supply chain
严选数十个优秀的医械行业服务机构,可为客户推荐更实惠的医械配套服务。
多次创造二三类高风险产品一次性通过的行业纪录
项目状态:已结案
项目辅导老师:李老师
项目状态:已结案
项目辅导老师:车老师
项目状态:已结案
项目辅导老师:王老师
项目状态:已结案
项目辅导老师:黄老师