在“一带一路”战略的引领下,东南亚医械市场成为我国医疗器械行业新的出口增长点,有数据显示,2022年东南亚市场已经占据我国医疗器械出口份额的30%以上,预计未来这个比例还将进一步上升。作为东南亚第二大经济体,泰国医疗器械市场的潜力不可小觑,今天就跟大家简单梳理一下泰国医疗器械注册的相关要点。
1. 查阅Risk classification of medical devices, B.E. 2562 (2019) 中提到的医疗器械/体外诊断试剂7条分类规则,依据分类规则判断产品风险等级;
2. 利用官网上的决策小工具You can check your devices' risk classification here by answering a few questions进行查询(具体网址可联系我们获取);
3. 在TFDA数据库Health Product Search中,用产品名称(英文/泰文)进行检索,查找类似产品在TFDA的分类,如下图。

【小知识点】:泰国医疗器械产品注册证编号的第三个数字为产品分类,例如65-1-3-2-0000172,则产品分类为Class 1。
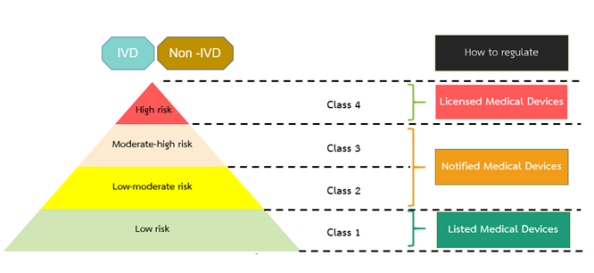
在泰国,Class 1的注册类型是Certificate of Listed(列名),Class 2 & 3的注册类型是Certificate of Notified(上市前通告),Class 4的注册类型则是Certificate of Licensed(上市前许可)。不同类别产品所需提交的注册资料不同,具体可联系我们咨询。
另外,对于Class 2~Class 4的医疗器械,TFDA证书有效期是5年,应在证书到期前或到期后一个月内提出续证申请并缴费;Class 1的证书则根据出口销售证明CFS确定。
确定产品在泰国属于医疗器械及相应的产品类别后,首要步骤就是指定泰国当地代理(establishment registrant),这一角色可以是自然人也可以是法人。而代理人在代表境外制造商办理相关医疗器械注册手续前,应先申请Establishment licence for importing,取得相应证照后,才能向TFDA提交注册申请,产品的注册证亦由代理人持有。

针对泰国当地代理,Medical Devices Act, B.E.2551 (2008) and (No. 2), B.E. 2562 (2019)的Section 16列出了11条要求,我们将其中前4条列举如下:
1. (申请medical device establishment的)企业所有人
2. 不低于20岁
3. 在泰国拥有住所
4. 没有破产
……
以上就是我们本期分享的泰国医疗器械注册的基本知识点,假如您有医疗器械海外(包括但不限于美国、欧盟、澳大利亚、加拿大、新加坡、日本、沙特等)注册需求,欢迎联系我们咨询!
医疗器械注册咨询认准金飞鹰 深圳:0755-86194173 广州:020 - 82177679 湖南:0731-22881823 四川:028 - 68214295


