
各有关单位:
为进一步提升标准制修订工作相关方参与程度,提高标准制修订工作质量与水平,本着公开、透明原则,我分技委现开展《医用内窥镜3D成像系统》等2项国家标准项目参与起草及验证单位征集工作,具体事项及相关要求如下:
一、标准项目清单
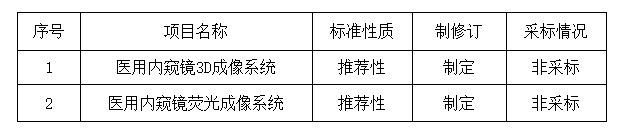
二、申请单位要求
1.业务范围与标准涉及的技术内容相适应,生产企业原则上应取得相关产品的注册证;
2.具有与制修订标准项目相关的研究、生产、检测、管理等工作背景和技术能力;
3.重视医疗器械标准化工作,熟悉医疗器械标准制修订工作流程,熟悉国家医疗器械有关政策、法规、标准的要求,了解标准中涉及的产品生产水平和使用要求、当前存在问题和解决方法、国内外技术发展趋势等;
4.具备独立法人资格,无任何违法、违规、失信等不良行为;
5.能够按标准制修订进度要求按时完成所承担的工作,如积极参与试验验证工作,提供代表性验证试验样品或承担验证试验任务等。
三、申报要求
申请参与起草单位请填写《医疗器械标准起草单位登记表》《医疗器械标准起草人登记表》(见附件1、附件2),申请标准验证单位请填写《医疗器械标准验证单位申请表》(附件3),盖章后于2026年4月24日前将电子版(PDF盖章版和word版)发送至秘书处邮箱。
四、秘书处联系方式
单位名称:浙江省医疗器械检验研究院 邮编:310018
联系人:夏忠诚 0571-86002820
邮箱:sactc103sc1@mdst.org.cn
五、其他说明
标准起草单位和起草人的署名将参照《国家标准委关于进一步规范推荐性国家标准起草单位和起草人署名的通知》(国标委发〔2025〕73号文)执行。
附件:
全国光学和光子学标准化技术委员会
医用光学和仪器分技术委员会
2026年4月17日

信息来源:中国食品药品检定研究院
排版整理:金飞鹰药械


