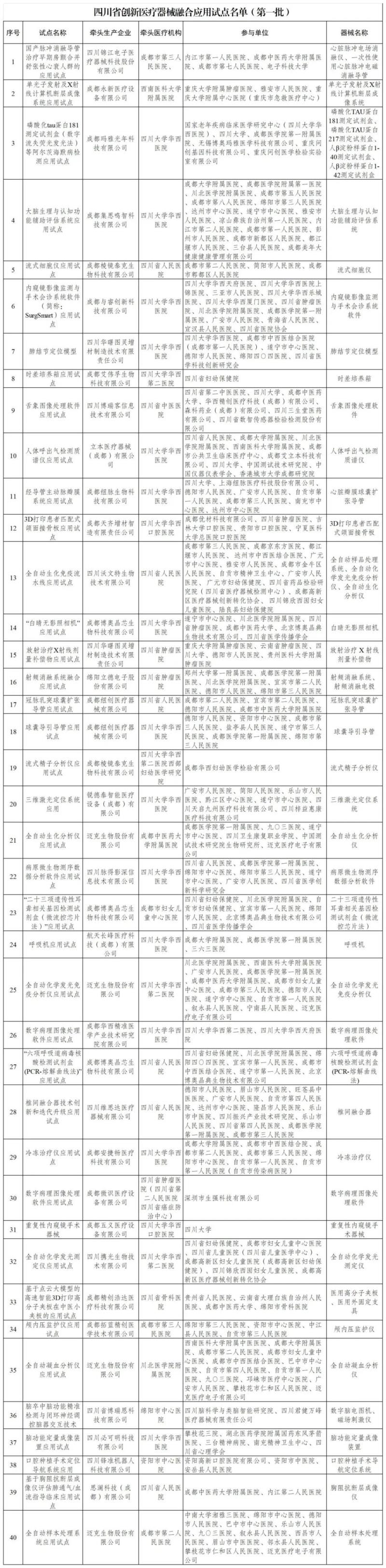
近日,四川省经济和信息化厅、四川省卫生健康委员会等8部门联合确定了《四川省创新医疗器械融合应用试点名单(第一批)》并予以公布,包括大脑生理与认知功能辅助评估系统、冷冻治疗仪、医用高分子夹板等器械产品,以下为具体明细:
据悉,这是依据2024年发布的《四川省推进创新医疗器械融合应用试点实施方案》(以下简称《方案》)开展的创新医疗器械融合应用试点申报工作。
《方案》申报方向及实施内容如下:
一、申报方向
(一)诊断检验仪器和试剂。
(二)治疗装备和器械。
(三)监护与生命支持装备。
(四)中医诊疗装备。
(五)保健康复装备。
(六)植介入及口腔医疗器械。
(七)智慧医疗、辅助诊断、移动医疗等。
(八)其他类医疗器械。
二、实施内容
应用试点是面向典型应用场景,在高端医疗器械技术创新与临床应用处于全国前列,对高端医疗器械医工协同创新、中试验证、临床应用研究、迭代升级与推广应用等具有较强的带动作用,应当包括但不限于:
(一)数据收集对比。对标同类先进产品的数据收集与对比。
(二)建立评价体系。建立创新医疗器械在医疗机构的使用规范和评价指标体系。
(三)修改完善提升。针对医疗机构提出的改进建议,提升医疗器械性能水平。
(四)组织人员培训。开展使用人员培训,培养应用人才。
(五)形成创新成果。形成医工融合创新成果,加快创新医疗器械应用。
➋ 未经审查发布医疗器械&处方药广告,广州一公司被罚42万! 医疗器械注册咨询认准金飞鹰 深圳:0755-86194173 广州:020 - 82177679 四川:028 - 68214295 湖南:0731-22881823 湖北:181-3873-5940 江苏:135-5494-7827 广西:188-2288-8311 海南:135-3810-3052 重庆:135-0283-7139


